Parodontologie
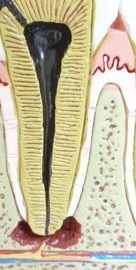
Das Parodontium besteht aus dem Zahnfleisch, dem Faserapparat, der den Zahn am Knochen fixiert und dem Wurzelzement des Zahnes. Dieser komplizierte Aufbau verhindert bei einem intakten Parodontium das Eindringen der Bakterien in den sog. Parodontalspalt.
Der Rückgang des Parodontiums wird als Parodontose, die Entzündung als Parodontitis bezeichnet. Die bakterielle Invasion führt zu einem Zersetzungsprozess des Faserapparates. Hierfür sind eine Fülle von Bakterien verantwortlich. Folgen der Bakteriellen Besiedlung ist die Zahnfleischentzündung (Gingivitis), die gekennzeichnet ist durch eine verstärkte Durchblutung. Das Zahnfleisch wird dicker, wölbt sich am Zahn empor und sorgt hier für eine Verstärkung der Entzündungen durch Schaffung neuer und tieferer Schmutznischen, die immer schwieriger zu reinigen sind. Die Folge ist das Zahnfleischbluten. Wenn die Bakterien den dichten Abschluß zum Faserapparat des Zahnes durchbrechen, erfolgt eine Entzündung des Parodontiums (Parodontitis). Der Faserapparat des Zahnes, das Zahnfleisch sowie der Kieferknochen werden geschädigt. Der Zahnhalteapparat wird abgebaut wodurch vermehrt Wurzeloberfläche frei liegt. Der Zahn reagiert nun sensibler auf Temperaturunterschiede. Die Wurzeloberfläche ist weicher als die Zahnkrone und damit anfälliger für bakterielle Zersetzungsprozesse, die sog. Wurzelkaries entsteht. Die Zähne verlieren durch den Rückgang des Alveolarfortsatzes ihre Fixierung im Knochen und beginnen dem Kaudruck auszuweichen, woraus ein Schmerz beim Kauen resultiert.
Die Parodontitis ist mit etwa 18 % eine der häufigsten Erkrankungen in Europa. In der Altersgruppe der 35 – 44 Jährigen liegt eine Erkrankungshäufigkeit von ca 73,2 % in Deutschland vor. Bei 20,5 % der Patienten liegt eine schwere Parodontitis vor. Eine unbehandelte Zahnbetterkrankung führt zu einem irreversiblen Attachmentverlust von ca. 0,2 mm pro Jahr. Ab dem 40. Lebensjahr gehen mehr Zähne durch Parodontitis als durch Karies verloren.
Die Parodontitis ist eine multifaktorielle Erkrankung. Die Hauptursache bildet die bakterielle Besiedlung der Zahnoberfläche in Folge unzureichender Mundhygiene. Faktoren wie Rauchen, Diabetes, Stress und genetische Vorgaben fördern die Erkrankung.
Die große Anzahl der dem Zahn und dem Zahnhalteapparat anhaftenden Bakterien können in die Blutbahn gelangen (Bakteriämie). Sie werden mit dem Blut an die verschiedenen Organe befördert, Die Folgen sind diabetes mellitus, koronare Herzerkrankungen, rheumatoide Arthritis und Schwangerschaftskomplikationen (Frühgeburten, niedriges Geburtsgewicht). Die Parodontitis fördert unter Umständen die Entstehung des Diabetes.
In der Mundhöhle befinden sich bis zu eine Billionen Bakterien aus mehr als 500 verschiedenen Spezies. Diese können ein komplexes Ökosystem entwickeln. Es gibt gute und böse Bakterien. Die guten Keime sind überwiegend grampositive aerobe Keime, die bösen Keime sind gramnegativ und anaerob. Der Biofilm, früher auch als Plaque bezeichnet, reizt das Zahnfleisch und führt zu dessen Entzündung. Schwellung, Entzündung und leichte Zahnfleischtaschen sind die Folgen. Im Zuge ihres Stoffwechsels scheiden die Bakterien zytotoxische Substanzen und proteolytische Enzyme aus. Diese zerstören aktiv das parodontale Gewebe wie Knochen und Weichgewebe. Der den Zahn im Knochen fixierende Faserapparat wird geschädigt mit dem Ergebnis der Zahnlockerung.
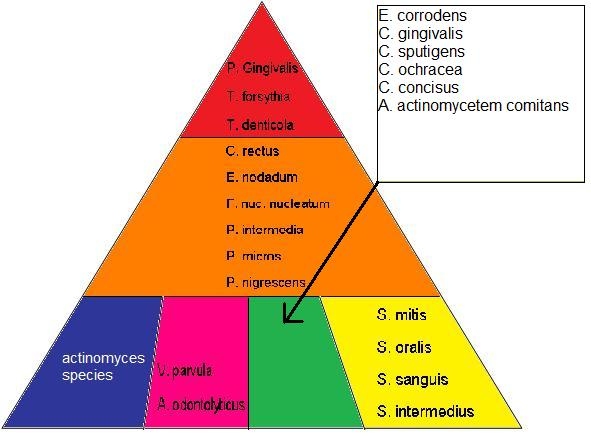
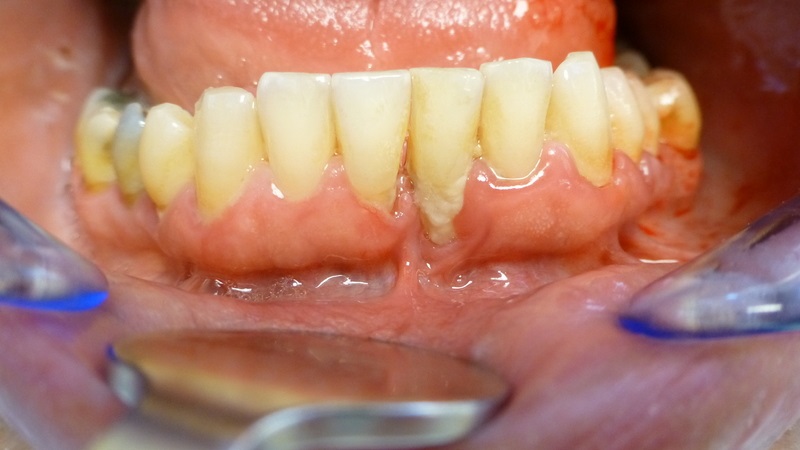
Das Ziel der Parodontalbehandlung liegt in der Reduktion der Keime und einer Wiederherstellung des Gleichgewichtes zwischen guten und bösen Bakterien.
- Veilonella parvula, Actinomyces ododntolyticus, C. rectus, E. nodatum C. showae, C. gracilis, S. constellatus sind Frühkolonialisierer mit geringen pathogenen Eigenschaften. Die erste Biofilmschicht wird durch diese Bakterien gebildet. Eine instrumentelle Therapie gilt als ausreichend. Bei sehr hohen Keimzahlen empfiehlt sich eine antibiotische Begleittherapie.
- Prevotella intermedia, Peptostreptococcus micros, Fusobakterium nucleatum fungieren als Brückenkeime zwischen den Frühkolianisierern und den pathogenen Keimen angesehen. Die Brückenkeime verursachen am Parodont einen fortschreitenden Attachmentverlust sowie eine zunehmende Taschentiefe. Durch ihre Stoffwechselprodukte sorgen sie für die Ansiedlung der gefährlichen anaeroben Keime in der Zahnfleischtasche. Bei niedriger Keimzahl empfiehlt sich eine mechanische Reinigung, bei hoher Keimzahl eine zusätzliche Therapie mittels Metronidazol (bei Abwesenheit von Actinobacillus actinomycetemcomitans) oder Clindamycin.
- Porphyromonas gingivalis, Treponema denticula und Tanerella forsythia produzieren proteolytische Enzyme wie Phosphatasen und Kollagenasen, die wiederum verstärkt den Knochen abbauen und das Weichgewebe auflösen. Als klinisches Bild erscheint die Taschentiefe, der Attachmentverlust und die Sondierungsblutung. Die Bakterien können sich der instrumentellen Therapie entziehen, indem sie sich im Epithel verstecken. Häufig ist eine antibiotische Therapie nicht zu umgehen ( Metronidazol, Clindamycin).
- Eikenella corrodens und Capnocytophaga sp. gelten als gering pathogen. Bei hohen Keimzahlen ist eine antibiotische Zusatztherapie (Amoxicillin, Ciprofloxacin) empfehlenswert. Der wichtigste Markeim für die iuvenile und aggressive Parodontitis ist Aggregatibacter actinomycetemcomitans. Dieser Keim produziert immunsuppressive Stoffe, hemmt also die körperliche Abwehr, und sorgt für eine vermehrte Freisetzung von Interleukin. Hierdurch wird der Knochenabbau beschleunigt. Eine rein instrumentelle Therapie reicht zur Behandlung nicht aus. Eine antibiotische Zusatztherapie mit Amoxicillin oder Ciprofloxacin wird erforderlich.
Die Parodontitis ist eine klassische Infektionskrankheit:
Eine mikrobiologische Untersuchung ist empfehlenswert bei
- aggressiver Parodontitis
- schweren chronischen Parodontitiden
- Parodontitiden, die trotz vorangegangener Therapie progrediente Attachmentverluste aufweisen
- mittelschwere bis schwere Parodontitiden bei systemischen Erkrankungen oder Zuständen, die die Funktion des Immunsystems negativ beeinflussen
Unser Immunsystem ist in der Lage auf diese bakterielle Schädigung zu reagieren. Der Wirkmechanismus der Bakterien auf unser Immunsystem ist sehr kompliziert. Die Bakterien exprimieren Lipopolysacchharidketten auf ihrer Oberfläche. Diese LPS Ketten werden durch das Immunsystems des Patienten erkannt. Diese Primärantwort besteht in einer Freisetzung von Zytokinen ( Interleukin-1, Interleukin-6, Interleukin 8 TNF )durch die Zellen des Zahnfleisches. Granulozyten wandern auf die Entzündung zu, fressen die Erreger auf und dämmen die Entzündung ein.
Wenn diese Abwehr ausbleibt, etabliert sich eine Parodontitis.
Die genetische Veranlagung kann einen entscheidenden Einfluss haben. Etwa ein Drittel der europäischen Bevölkerung weist dieses genetische Merkmal auf. Hier spielen das Interleukin-1A (IL-1A) und Interleukin-1B (IL-1B)und deren Genegenspieler, der Interleukin-1-Rezeptorantagonist (IL-1RN) eine wichtige Rolle. IL-1 aktiviert Knochen aufbauende Zellen, während Knochen aufbauende Zellen deaktiviert werden. Hieraus resultiert ein Knochenschwund. Durch den Gendefekt entsteht ein signifikant höherer Knochenabbau sofern eine bakterielle Entzündung vorhanden ist . Zudem liegt bei diesen Menschen eine erhöhte Entzündungsneigung vor. Wenn eine genetische Veränderung des Rezeptors vorhanden ist, kann durch eine nicht mehr optimale Blockierung diese Rezeptors eine abgeschwächte Immunantwort ergeben. Diese IL-1 vermittelte Immunantwort kann durch molekulargenetische Untersuchungen bestimmt werden.
Das Zusammenspiel der unterschiedlichen Bakterien führt bei bestehendem Ungleichgewicht und genetischer Disposition zur Parodontitis.
Ernährungsberatung in Parodontosefällen und Fällen von reduziertem Zahnbestand:
Eine mangelhafte Vitamin-C-Versorgung erhöht das Risiko für eine Parodantitis
- wasserlösliches Vitamin
- wird durch frische pflanzliche Nahrung aufgenommen
- vorhanden in Beeren, Zitrusfrüchten, Gemüse, Fenchel, Paprika
- es wird beim Garen zum Großteil zerstört, da es hitzelabil ist
- geeignet für den Rohverzehr
Zubereitung der Nahrung bei eingeschränkter Nahrungszerkleinerung:
- Pürieren von frischem Obst
- Herstellung frisch gepresster Obstsäfte
- Vitaminschonende Zubereitungsart durch Dünsten in wenig Flüssigkeit und Garen verschiedener Gemüsesorten im Wok
- Raspeln von Möhren, roter Beete oder Äpfeln ermöglicht den Verzehr von Rohkost
- Nüsse können in Form von Nussmus als Brotaufstrich dienen